· El hierro y el acero que se utilizan para hacer los imanes y la carcasa del motor, que tienen una fabricación especifica, como podemos observar en el dibujo siguiente:


Propiedades y estado natural
Se prepara en forma de polvo amorfo amarillo pardo o de cristales negros-grisáceos. Se obtiene calentando sílice, o dióxido de silicio (SiO2), con un agente reductor, como carbono o magnesio, en un horno eléctrico. El silicio cristalino tiene una dureza de 7, suficiente para rayar el vidrio, de dureza de 5 a 7. El silicio tiene un punto de fusión de 1.410 °C, un punto de ebullición de 2.355 °C y una densidad relativa de 2,33. Su masa atómica es 28,086.
Se disuelve en ácido fluorhídrico formando el gas tetrafluoruro de silicio, SiF4 (véase Flúor), y es atacado por los ácidos nítrico, clorhídrico y sulfúrico, aunque el dióxido de silicio formado inhibe la reacción. También se disuelve en hidróxido de sodio, formando silicato de sodio y gas hidrógeno. A temperaturas ordinarias el silicio no es atacado por el aire, pero a temperaturas elevadas reacciona con el oxígeno formando una capa de sílice que impide que continúe la reacción. A altas temperaturas reacciona también con nitrógeno y cloro formando nitruro de silicio y cloruro de silicio respectivamente.
El silicio constituye un 28% de la corteza terrestre. No existe en estado libre, sino que se encuentra en forma de dióxido de silicio y de silicatos complejos. Los minerales que contienen silicio constituyen cerca del 40% de todos los minerales comunes, incluyendo más del 90% de los minerales que forman rocas volcánicas. El mineral cuarzo, sus variedades (cornalina, crisoprasa, ónice, pedernal y jaspe) y los minerales cristobalita y tridimita son las formas cristalinas del silicio existentes en la naturaleza. El dióxido de silicio es el componente principal de la arena. Los silicatos (en concreto los de aluminio, calcio y magnesio) son los componentes principales de las arcillas, el suelo y las rocas, en forma de feldespatos, anfíboles, piroxenos, micas y ceolitas, y de piedras semipreciosas como el olivino, granate, zircón, topacio y turmalina.
Aplicaciones
Se utiliza en la industria del acero como componente de las aleaciones de silicio-acero. Para fabricar el acero, se desoxida el acero fundido añadiéndole pequeñas cantidades de silicio; el acero común contiene menos de un 0,03% de silicio. El acero de silicio, que contiene de 2,5 a 4% de silicio, se usa para fabricar los núcleos de los transformadores eléctricos, pues la aleación presenta baja histéresis (véase Magnetismo). Existe una aleación de acero, el durirón, que contiene un 15% de silicio y es dura, frágil y resistente a la corrosión; el durirón se usa en los equipos industriales que están en contacto con productos químicos corrosivos. El silicio se utiliza también en las aleaciones de cobre, como el bronce y el latón.
El silicio es un semiconductor; su resistividad a la corriente eléctrica a temperatura ambiente varía entre la de los metales y la de los aislantes. La conductividad del silicio se puede controlar añadiendo pequeñas cantidades de impurezas llamadas dopantes. La capacidad de controlar las propiedades eléctricas del silicio y su abundancia en la naturaleza han posibilitado el desarrollo y aplicación de los transistores y circuitos integrados que se utilizan en la industria electrónica.
La sílice y los silicatos se utilizan en la fabricación de vidrio, barnices, esmaltes, cemento y porcelana, y tienen importantes aplicaciones individuales. La sílice fundida, que es un vidrio que se obtiene fundiendo cuarzo o hidrolizando tetracloruro de silicio, se caracteriza por un bajo coeficiente de dilatación y una alta resistencia a la mayoría de los productos químicos. El gel de sílice es una sustancia incolora, porosa y amorfa; se prepara eliminando parte del agua de un precipitado gelatinoso de ácido silicio, SiO2·H2O, el cual se obtiene añadiendo ácido clorhídrico a una disolución de silicato de sodio. El gel de sílice absorbe agua y otras sustancias y se usa como agente desecante y decolorante.
El silicato de sodio (Na2SiO3), también llamado vidrio, es un silicato sintético importante, sólido amorfo, incoloro y soluble en agua, que funde a 1.088 °C. Se obtiene haciendo reaccionar sílice (arena) y carbonato de sodio a alta temperatura, o calentando arena con hidróxido de sodio concentrado a alta presión. La disolución acuosa de silicato de sodio se utiliza para conservar huevos; como sustituto de la cola o pegamento para hacer cajas y otros contenedores; para unir gemas artificiales; como agente incombustible, y como relleno y adherente en jabones y limpiadores. Otro compuesto de silicio importante es el carborundo, un compuesto de silicio y carbono que se utiliza como abrasivo.
El monóxido de silicio, SiO, se usa para proteger materiales, recubriéndolos de forma que la superficie exterior se oxida al dióxido, SiO2. Estas capas se aplican también a los filtros de interferencias.
· El Aluminio, de símbolo Al, es el elemento metálico más abundante en la corteza terrestre. Su número atómico es 13 y se encuentra en el grupo 13 de la tabla periódica.
El químico danés Hans Christian Oersted aisló el aluminio por primera vez en 1825, por medio de un proceso químico que utilizaba una amalgama de potasio y cloruro de aluminio. Entre 1827 y 1845, el químico alemán Friedrich Wöhler mejoró el proceso de Oersted utilizando potasio metálico y cloruro de aluminio. Wöhler fue el primero en medir la densidad del aluminio y demostrar su ligereza. En 1854, Henri Sainte-Claire Deville obtuvo el metal en Francia reduciendo cloruro de aluminio con sodio. Con el apoyo financiero de Napoleón III, Deville estableció una planta experimental a gran escala, y en la exposición de París de 1855 exhibió el aluminio puro.
Propiedades
El aluminio es un metal plateado muy ligero. Su masa atómica es 26,9815; tiene un punto de fusión de 660 ºC, un punto de ebullición de 2.467 ºC y una densidad relativa de 2,7. Es un metal muy electropositivo y muy reactivo. Al contacto con el aire se cubre rápidamente con una capa dura y transparente de óxido de aluminio que resiste la posterior acción corrosiva. Por esta razón, los materiales hechos de aluminio no se oxidan. El metal reduce muchos compuestos metálicos a sus metales básicos. Por ejemplo, al calentar termita (una mezcla de óxido de hierro y aluminio en polvo), el aluminio extrae rápidamente el oxígeno del óxido; el calor de la reacción es suficiente para fundir el hierro. Este fenómeno se usa en el proceso Goldschmidt o Termita para soldar hierro (véase Soldadura).
Entre los compuestos más importantes del aluminio están el óxido, el hidróxido, el sulfato y el sulfato mixto. El óxido de aluminio es anfótero, es decir, presenta a la vez propiedades ácidas y básicas. El cloruro de aluminio anhidro es importante en la industria petrolífera. Muchas gemas (el rubí y el zafiro, por ejemplo) consisten principalmente en óxido de aluminio cristalino.
El aluminio es el elemento metálico más abundante en la corteza terrestre; sólo los no metales oxígeno y silicio son más abundantes. Se encuentra normalmente en forma de silicato de aluminio puro o mezclado con otros metales como sodio, potasio, hierro, calcio y magnesio, pero nunca como metal libre. Los silicatos no son menas útiles, porque es extremamente difícil, y por tanto muy caro, extraer el aluminio de ellas. La bauxita, un óxido de aluminio hidratado impuro, es la fuente comercial de aluminio y de sus compuestos.
En 1886, Charles Martin Hall en Estados Unidos y Paul L. T. Héroult en Francia descubrieron por separado y casi simultáneamente que el óxido de aluminio o alúmina se disuelve en criolita fundida (Na3AlF6), pudiendo ser descompuesta electrolíticamente para obtener el metal fundido en bruto. El proceso Hall-Héroult sigue siendo el método principal para la producción comercial de aluminio, aunque se están estudiando nuevos métodos. La pureza del producto se ha incrementado hasta un 99,5% de aluminio puro en un lingote comercialmente puro; más tarde puede ser refinado hasta un 99,99 por ciento.
Aplicaciones
Un volumen dado de aluminio pesa menos que 1/3 del mismo volumen de acero. Los únicos metales más ligeros son el litio, el berilio y el magnesio. Debido a su elevada proporción resistencia-peso es muy útil para construir aviones, vagones ferroviarios y automóviles, y para otras aplicaciones en las que es importante la movilidad y la conservación de energía. Por su elevada conductividad térmica, el aluminio se emplea en utensilios de cocina y en pistones de motores de combustión interna. Solamente presenta un 63% de la conductividad eléctrica del cobre para alambres de un tamaño dado, pero pesa menos de la mitad. Un alambre de aluminio de conductividad comparable a un alambre de cobre es más grueso, pero sigue siendo más ligero que el de cobre. El peso tiene mucha importancia en la transmisión de electricidad de alto voltaje a larga distancia, y actualmente se usan conductores de aluminio para transmitir electricidad a 700.000 voltios o más.
El metal es cada vez más importante en arquitectura, tanto con propósitos estructurales como ornamentales. Las tablas, las contraventanas y las láminas de aluminio constituyen excelentes aislantes. Se utiliza también en reactores nucleares a baja temperatura porque absorbe relativamente pocos neutrones. Con el frío, el aluminio se hace más resistente, por lo que se usa a temperaturas criogénicas. El papel de aluminio de 0,018 cm de espesor, actualmente muy utilizado en usos domésticos, protege los alimentos y otros productos perecederos. Debido a su poco peso, a que se moldea fácilmente y a su compatibilidad con comidas y bebidas, el aluminio se usa mucho en contenedores, envoltorios flexibles, y botellas y latas de fácil apertura. El reciclado de dichos recipientes es una medida de conservación de la energía cada vez más importante. La resistencia a la corrosión al agua del mar del aluminio también lo hace útil para fabricar cascos de barco y otros mecanismos acuáticos.
Se puede preparar una amplia gama de aleaciones recubridoras y aleaciones forjadas que proporcionen al metal más fuerza y resistencia a la corrosión o a las temperaturas elevadas. Algunas de las nuevas aleaciones pueden utilizarse como planchas de blindaje para tanques y otros vehículos militares.
Producción
La producción mundial de aluminio ha experimentado un rápido crecimiento, aunque se estabilizó a partir de 1980. En 1900 esta producción era de 7.300 toneladas, en 1938 de 598.000 toneladas y en 1994 la producción de aluminio primario fue de unos 19 millones de toneladas. Los principales países productores son Estados Unidos, Rusia, Canadá, China y Australia.
· El Imán, sustancia que, por condición natural o adquirida, tiene la propiedad de atraer al hierro.
La magnetita o piedra imán es un imán natural compuesto, fundamentalmente, de óxido de hierro (Fe3O4). Se puede imanar un trozo de hierro sometiéndolo a un campo magnético creado por un imán o por una corriente eléctrica (véase Magnetismo). El hierro dulce (hierro con muy bajo contenido en carbono) se convierte en un imán artificial que pierde su magnetismo cuando deja de estar en contacto con el primer imán (o, como en el caso de un electroimán, cuando deja de pasar la corriente eléctrica por el arrollamiento conductor). El acero imanado es un imán artificial permanente porque sí conserva su magnetismo.
Si un imán se coloca entre limaduras de hierro, éstas se agrupan alrededor de sus extremos o polos, llamados polo norte y polo sur. Si se fragmenta un imán, cada fragmento presenta de nuevo un polo norte y un polo sur.
· Producción del cobre:
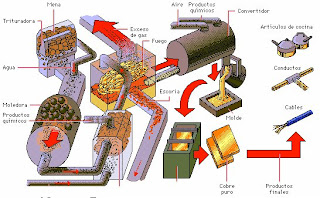
Los yacimientos de cobre contienen generalmente concentraciones muy bajas del metal. Ésta es la causa de que muchas de las distintas fases de producción tengan por objeto la eliminación de impurezas. La mena de cobre se tritura y muele antes de ser introducida en una cámara de flotación, en la que el cobre se concentra en la superficie, mientras los fragmentos sobrantes se hunden. Después, el concentrado, que se denomina carga, se introduce en un horno de reverbero que separa más impurezas. Durante el proceso de fundición, se extraen los gases de desecho, y el material forma en el fondo del horno un charco de hierro y cobre fundidos, llamado mata. La capa anaranjada de metal impuro en la superficie de la mata es escoria, que se drena y extrae mientras la mata de cobre sigue su proceso en un convertidor. El cobre fundido del convertidor es moldeado, y debe ser refinado una vez más por electrólisis antes de utilizarse para la fabricación de productos como cables eléctricos y herramientas.
· Los plásticos, generalmente derivados del petróleo, se producen artificialmente por procedimientos químicos.
Se puede decir que hoy todo se puede fabricar en plástico: muebles, lanchas, envases de todo tipo, viviendas, etc. Muchisimas piezas, que siempre se hicieron de acero, son sustituidas por piezas de plástico y, en muchos casos, con ventaja.




